Jean-Louis SCHLIENGER, Strasbourg
Blüher M et al. Dose-response effects on HbA1c and bodyweight reduction of survodutide, a dual glucagon/GLP‑1 receptor agonist, compared with placebo and open‑label semaglutide in people with type 2 diabetes: a randomised clinical trial. Diabetologia 2023 ; 67 : 470-82.
Hormone contre-régulatrice de l’insuline, le glucagon a la capacité de stimuler la glycogénolyse et la gluconéogenèse, ce qui lui confère un effet hyperglycémiant utilisé depuis des lustres pour corriger l’hypoglycémie sévère. Plus confidentiel, l’effet chronotrope du glucagon est utilisé pour traiter certaines bradycardies. Enfin, oubliés jusqu’à peu, des effets bénéfiques du glucagon sur la masse grasse corporelle, la prise alimentaire et la dépense énergétique avaient été décrits par les physiologistes. Et voici que le glucagon est proposé pour traiter l’obésité et même le diabète de type 2, ce qui peut paraître contre-intuitif. Dans un essai de phase 2, le rétatrutide, triple agoniste des récepteurs GLP-1, GIP et glucagon s’était avéré plus performant que le dulaglutide en termes de diminution de poids et d’HbA1c. Cet avantage avait été attribué à l’augmentation de la dépense énergétique induite par les agonistes des récepteurs du glucagon.
Dans cet essai de phase 2 randomisé, en double aveugle, contrôlé par placebo, l’efficacité du survodutide (BI 456906), double agoniste du récepteur du glucagon et du GLP-1, a été évaluée dans la prise en charge de l’obésité non compliquée par un diabète. L’essai multicentrique (12 pays, 43 centres) a été mené chez 387 sujets âgés de 18 à 75 ans ayant un surpoids ou une obésité (IMC moyen = 37,1 kg/m2). Une injection sous-cutanée hebdomadaire de survodutide (0,6, 2,4, 3,6 ou 4,8 mg) ou de placebo a été effectuée pendant 46 semaines (20 semaines d’augmentation de la dose ; 26 semaines de maintien de la dose). Le critère de jugement principal était le pourcentage de variation du poids corporel observé à la fin de l’essai. Des analyses de sensibilité et d’innocuité chez tous les sujets ayant reçu au moins une dose ont complété les résultats. À l’issue des 46 semaines, la perte de poids moyenne était proportionnelle à la dose survodutide : -6,2 ; -12,5 ; -13,2 et -14,9 % selon la dose croissante de survodutide contre -2,8 % sous placebo et 98 % des sujets ont perdu au moins 5 % du poids initial vs 4 % dans le groupe placebo. Une perte > 20 % a été obtenue chez 33 % des sujets à la dose maximale (figure). Une diminution significative de la pression artérielle, des triglycérides des transaminases et de l’HbA1c a été observée chez tous les patients sous survodutide. Des effets indésirables ont été recensés chez 91 % des patients sous traitement actif et 75 % sous placebo avec une prépondérance d’effets digestifs (respectivement 75 et 42 %) à type de nausées, vomissements, diarrhée ou constipation. Seuls 10 % ont été qualifiés de sévères (7 % sous placebo).
Dans cette étude de phase 2, un double analogue du récepteur du glucagon et du GLP-1 a entraîné une perte de poids conséquente dose-dépendante, chez des sujets obèses non diabétiques. A la dose maximale de 4,8 mg, la perte de poids était au moins égale à celle obtenue sous sémaglutide 2,4 mg, analogue du récepteur du GLP-1 qui fait référence, et proche de celle rapportée avec le tirzépatide, double agoniste des récepteurs GLP-1 et GIP. La tolérance était comparable à celle des autres analogues de type « dutide ». En dépit des limites méthodologiques inhérentes aux essais de phase 2 – durée relativement courte, effectif restreint dans chaque groupe, absence de comparateur actif –, la combinaison d’un analogue du récepteur du glucagon à un analogue des récepteurs d’incrétine paraît prometteuse dans le traitement de l’obésité et du DT2. C’est la confirmation du renouveau du glucagon dans un rôle inattendu !
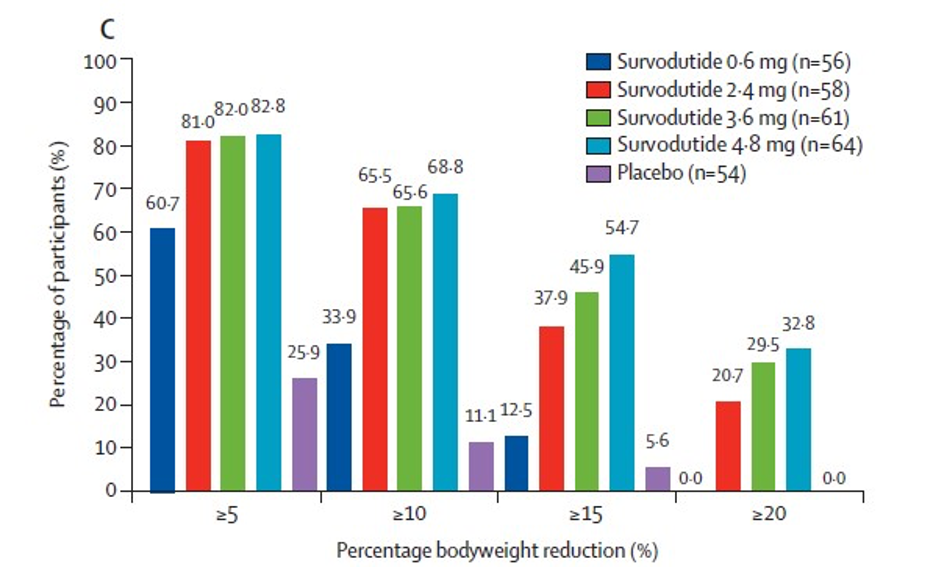
Figure. Pourcentage de participants ayant perdu au moins 5, 10, 15 ou 20 % du poids initial après 46 semaines de traitement à différentes posologies de survodutide.